发布日期:2026-2-22 9:52:09
随着骨科疾病发病率不断上升及精准医学理念的深入发展,临床对个性化、高匹配度骨科植入物的需求日益迫切。钛合金凭借其高强度、优良生物相容性和耐腐蚀性能,长期占据骨科植入材料的主导地位,但传统制造技术在复杂解剖结构成形、个体化匹配及微观结构精准调控方面逐渐暴露出局限性。近年来,选区激光熔化 (SLM) 和电子束熔化 (EBM) 等增材制造技术依托数字化设计和逐层成形机制,实现了多孔结构、功能梯度材料及复杂几何体的精确构筑,在改善力学匹配性和促进骨整合方面表现出显著优势,但在表面粗糙度控制及孔隙结构与力学性能的协同优化方面仍面临挑战。在此基础上,人工智能被引入钛合金增材制造与骨科植入材料研究中,作为贯穿设计 - 制造 - 评价 - 临床预测全过程的核心工具:在设计阶段,AI 通过拓扑优化与生成式算法实现轻量化、多孔及梯度化结构设计,以缓解弹性模量失配和应力遮挡;在制造阶段,机器学习与深度学习用于实时监测 SLM 过程中的熔池及多物理信号,实现缺陷识别与工艺自适应调控;在评价与应用层面,AI 将 SLM 制备的 Ti-6Al-4V (Ti64) 实验数据与有限元力学 - 生物学骨愈合模型相结合,揭示结构 - 性能 - 骨愈合之间的非线性关系,实现骨再生与长期稳定性的快速预测,从而推动钛合金骨科植入物向智能化、精准化和个性化方向发展。本文系统地梳理钛合金增材制造在骨科中的应用研究进展,比较不同技术路线的优劣,旨在为下一代植入物的创新设计与临床转化提供依据,推动骨科植入材料的技术革新与临床应用拓展。
1、钛合金材料特性与骨科适配性
1.1 力学匹配性
Ti6A14V (E≈110 GPa) 因强度优异被广泛用于骨科植入,但其刚度约为皮质骨 (10~30GPa) 的 3~10 倍,不可避免地引发应力遮蔽。植入物承担大部分载荷后,周围骨应变骤降,长期导致骨量丢失、吸收及无菌性松动。为缩小模量差距,研究同步推进成分设计与结构工程,主要技术策略包括合金化处理基体和多孔化结构设计两方面。(1) 合金化:添加 Nb、Zr 等 β 稳定元素可获得单一 β 相,显著降低弹性模量。Ozan 等报道的 Ti–Nb–Zr 合金 E=62 ~ 65 GPa,屈服强度 700MPa 级,延伸率 > 10%,弹性应变 1.31%;高 Zr 含量还抑制磷酸钙过度沉积,维持成骨细胞活性,兼顾应力遮蔽缓解与后期取出需求。(2) 多孔化:通过增材制造调控孔隙率可进一步下调表观模量。Devaraj 等采用 SLM 制备孔隙率 20~40% 的 Ti6Al4V,30% 孔隙试样 E≈60GPa,与松质骨接近。Murr 等利用 EBM 构建 60~80% 孔隙结构,模量降至 40~80GPa,同时提供三维互通空间,利于骨长入与血管化,促进骨整合。综上,成分 - 结构协同策略可将钛合金有效模量调至骨水平,为开发力学 - 生物学性能兼优的新一代植入物提供可行途径。
1.2 生物相容性
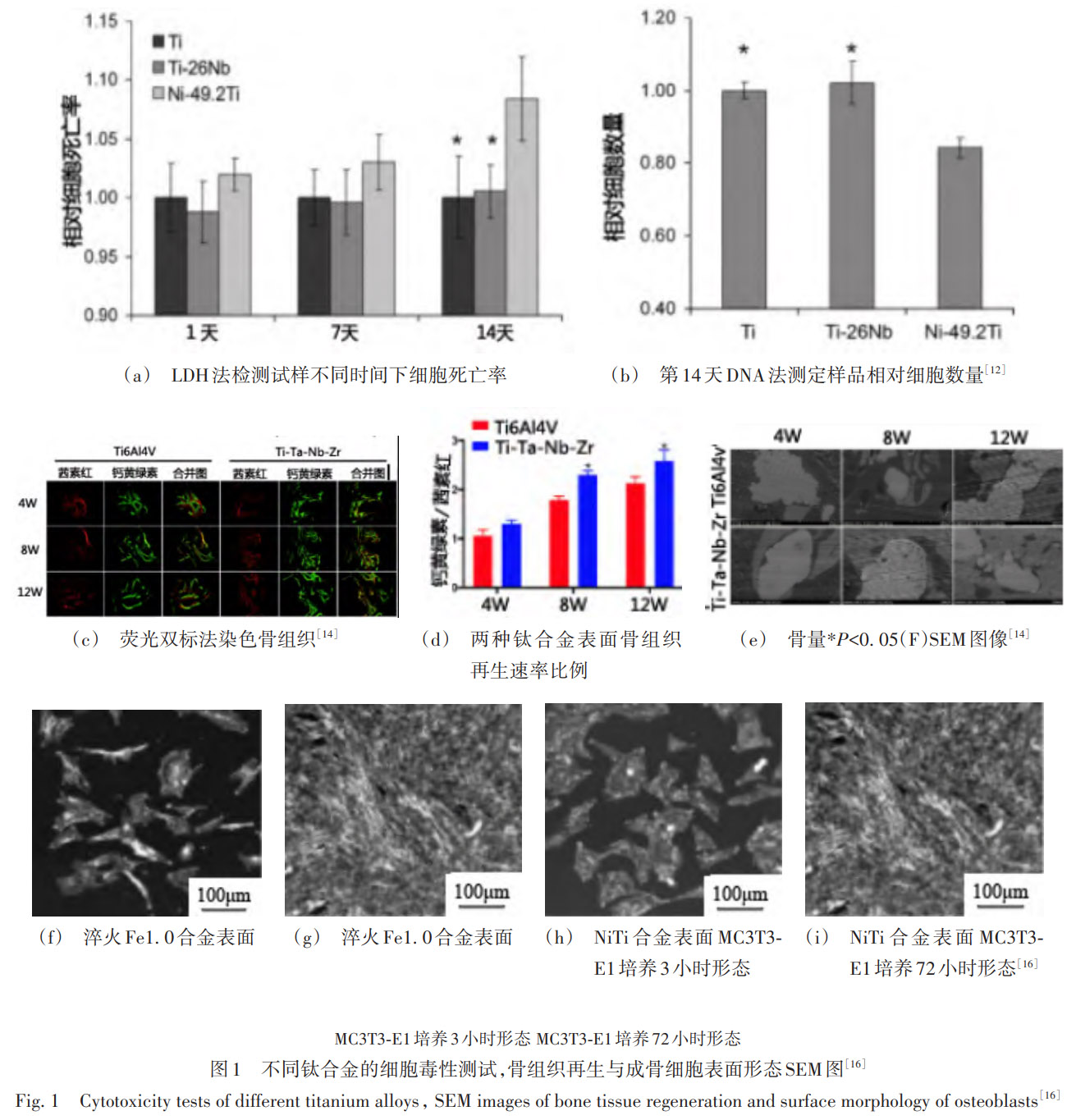
钛合金的骨床应用根基在于其卓越的生物相容性:不仅可规避宿主免疫排斥,还能主动诱导骨原细胞附着与向心性长入。为了突破 Ti6Al4V 固有性能的极限,近期研究采用 “成分 - 结构 - 表面” 三元协同策略,系统提升骨整合效率。McMahon 等在系统比较了 Ni-49.2Ti 与 Ti-26Nb 形状记忆合金的细胞相容性与耐腐蚀行为,采用三维 PEGDA 水凝 胶包埋 NIH3T3 成纤维细胞的间接体外培养模型,通过乳酸脱氢酶 (LDH) 释放与 DNA 含量评估细胞毒性,同时结合电化学动电位极化测试、ICP-MS 离子释放分析及 SIMS 表面成分深度剖析,全面表征材料在类生理环境中的反应行为。研究结果显示,Ti-26Nb 合金在整个培养周期内的细胞毒性水平与纯钛相当,而 NiTi 合金在长期培养 (14d) 后表现出更高的 LDH 释放和显著降低的 DNA 含量,显示出较强的细胞毒性。该差异主要归因于 NiTi 合金较高的镍离子释放和较低的耐腐蚀稳定性;相较之下,Ti-26Nb 合金由于 Ti 与 Nb 均能形成稳定的钝化氧化膜,其离子溶出显著降低、耐蚀性更优,从而表现出更好的生物相容性。Liu 等利用激光粉末床熔融 (LPBF) 实现 Ti-Ta 原位合金化,所得材料疲劳极限较纯钛提升 35%;兔股骨缺损模型 12 周后骨 - 植入物接触率 (BIC) 达 40%,为纯钛组 1.9 倍,预示优异的临床转化应用前景。Guo 等通过选区激光熔化 (SLM) 构筑孔隙率 60%、孔径 300~400µ 的 Ti-Ta-Nb-Zr 支架,表观模量降至 2.34GPa,与松质骨高度匹配;体外实验显示,人骨髓间充质干细胞 (hBMSCs) 在其表面黏附率提高 30%,ALP 活性提升 1.8 倍;兔股骨髁缺损 12 周新骨体积分数达 45%,证实同步降低应力遮蔽并加速骨整合。Jing 等则采用 PLGA - 辛伐他汀水凝胶涂层覆于 SLM 钛支架,21 天累计释放,经 TF / NOX₂通路诱导骨肉瘤细胞凋亡率 65%,同时使 hBMSCs 钙结节沉积增加 50%,大鼠股骨感染率由 30% 降至 5%。Xue 等围绕钛合金在人体中的生物相容性问题,制备并系统研究了一种无镍超弹性 Ti-19Zr-10Nb-1Fe 合金。通过合金熔炼与热处理获得 β 型组织,采用电化学极化测试和离子释放实验评估其在模拟体液中的耐腐蚀行为与金属离子溶出特性,并结合成骨细胞体外培养实验、溶血实验及血小板黏附 / 激活测试,全面表征其细胞相容性与血液相容性。结果表明,该钛合金在 Hank’s 溶液中表现出更低的腐蚀速率和显著降低的离子释放量,成骨细胞黏附与增殖性能与 NiTi 合金相当,但在溶血率和血小板激活程度方面明显优于 NiTi。得出结论 Ti-19Zr-10Nb-1Fe 合金凭借低毒元素组成、优良耐蚀性及良好的细胞与血液相容性,展现出作为新一代高生物相容性医用钛合金、替代传统 NiTi 合金的潜在应用价值。Li 等设计 55% 孔隙率的方形杆状多孔 Ti6Al4V,计算流体动力学表明其剪切应力通过 Piezo1/YAP 信号轴显著促进增殖 (7 ~d OD ≈1.8)。压缩强度约 280MPa 接近皮质骨;兔膝关节缺损 12 周软骨层厚度达 0.8mm,较均孔支架增厚 30%。综上,成分优化、多级孔结构及药物缓释涂层的协同集成,使新一代钛合金植入物在力学适配、骨整合速率与抗感染性能上实现同步跃升,为复杂骨科缺损修复提供了极具竞争力的综合解决方案。
1.3 耐腐蚀性
钛合金表面自发生成的纳米级 TiO₂氧化膜赋予其在生理环境中优异的化学稳定性,长期服役仍保持低腐蚀速率。为了进一步提升耐蚀极限,表面改性已成为关键突破口。Chelappa 等采用电泳沉积技术在表面构筑 SiO₂-ZnO 复合涂层,并以 I₂PVP 协同致密化结构;模拟体液中,涂层使腐蚀电位升至,腐蚀电流密度降至 5.1 ×10⁻² m・A・cm⁻²,耐蚀性显著提高,且涂层基体结合强度达 45MPa,兔股骨植入 6 周后界面骨整合率提升 25%。Xie 等发现,3D 打印 Ti6Al4V 表面的部分熔化颗粒 (PMCs) 破坏氧化膜完整性,Cl⁻渗透速率提高,腐蚀电流密度增至 1.8 ×10⁻⁶ A・cm⁻²(为无 PMCs 表面的 2.3 倍);将激光功率从 180W 提高至 220W 后,PMCs 面积分数由 12% 降至 3%,点蚀电位自 0.6V 升至 1.1V,耐蚀性能恢复。Guo 等利用 3D 打印制备 TiCu/Ti-Cu-N 涂层支架,XPS 证实 Cu 以 Cu⁰/Cu²⁺共存,生理环境中持续释放 Cu²⁺(0.45 μg・cm⁻²・d⁻¹),抑制大肠杆菌粘附,并与 TiO₂氧化层协同形成复合保护膜,使中的腐蚀电位自提升至 1.3V。综上,通过成分设计、工艺参数优化与功能涂层协同,可同步强化钛合金植入物的耐蚀性与生物活性,为延长服役寿命并降低感染风险提供新策略。
2、增材制造技术关键工艺与挑战
2.1 核心技术原理
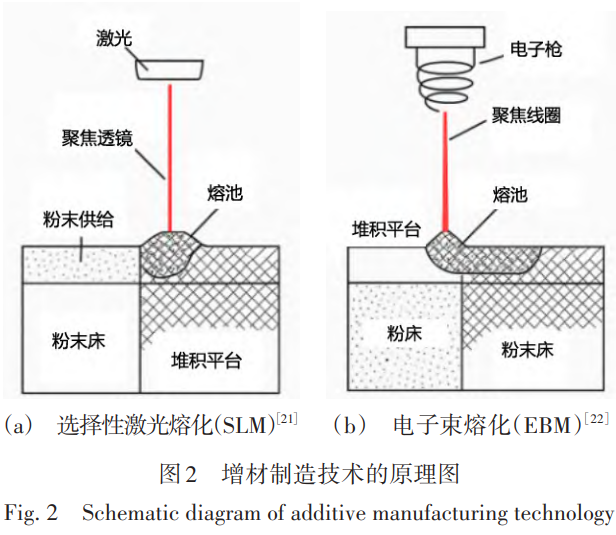
增材制造技术为钛合金植入物的生产提供了新途径,其中选择性激光熔化 (SLM) 和电子束熔化 (EBM) 是两种主流的粉末床熔融方法。两者基本原理相似,均通过高能束流 (激光或电子束) 在金属粉末床上逐层选择性熔化材料,实现逐层堆积成型。SLM 采用高功率光纤激光器作为能量源,在惰性气体保护下熔化金属粉末,具有较高的成形精度和表面质量。而 EBM 则利用高能电子束作为热源,在高真空环境中熔化金属粉末,具备熔化速度快、残余应力控制良好的优势。
2.2 SLM 与 EBM 的对比
增材制造相较传统减材工艺可一次成形复杂拓扑与个体化植入物,显著降低材料损耗并压缩生产周期。EBM 凭借高温平台及缓慢冷却在耐蚀性与生物活性上优于 SLM,而 SLM 则因高冷速获得更高力学强度。Zhao 等报道,SLM 冷却速率约 10³ ~ 10⁸℃・s⁻¹,生成针状 α' 马氏体,抗拉强度 980MPa,延伸率 8%;EBM 预热≈700℃、冷速 10~10²℃・s⁻¹,形成柱状 β 晶及 a 板条,强度 920MPa,但延伸率 12%。
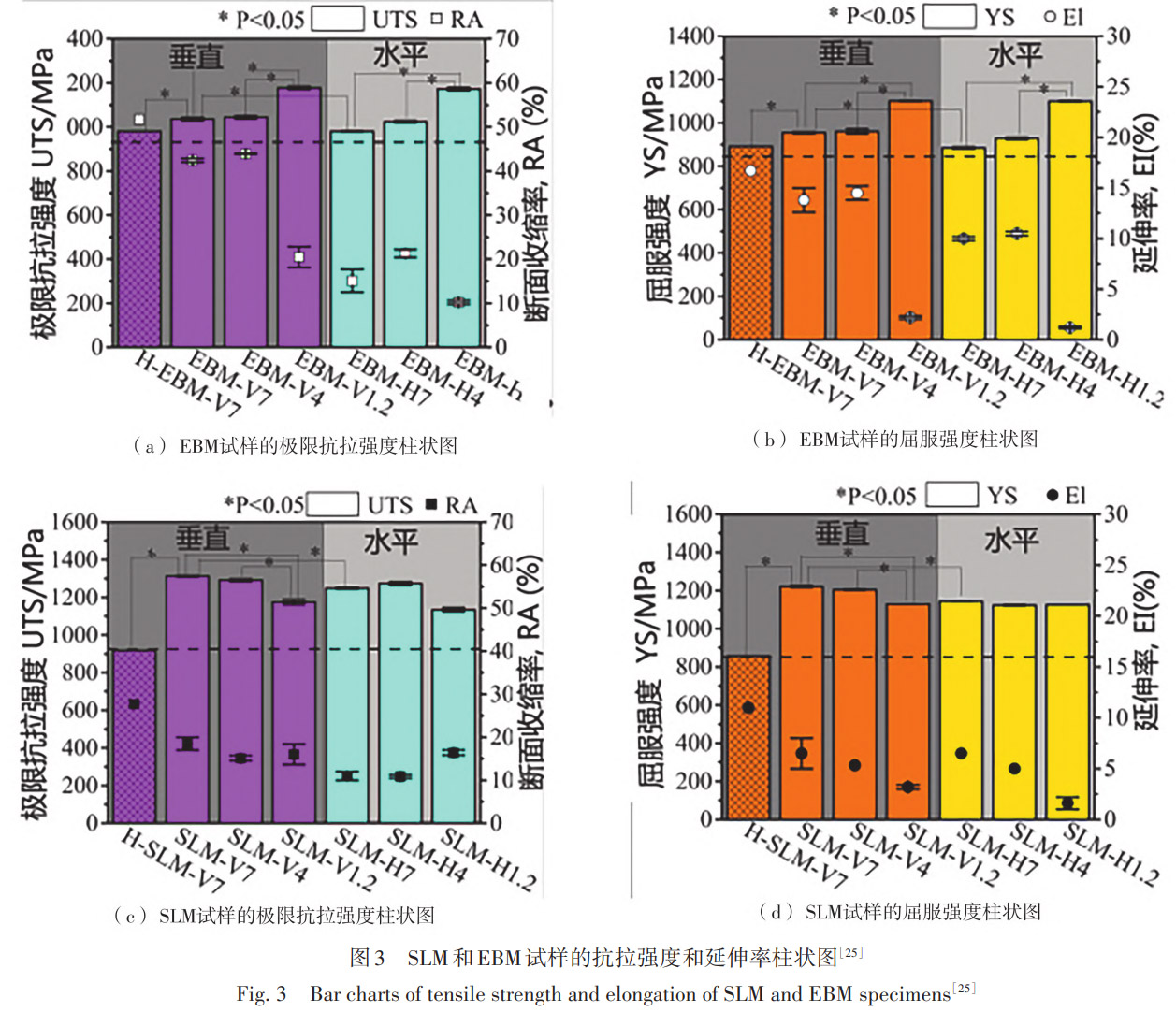
Pasang 等系统对比了 SLM 与 EBM 制备 Ti6Al-4V 在不同成形方向 (0°、45°、90°) 下的组织与力学性能差异。采用选择性激光熔化 (SLM) 与电子束熔化 (EBM) 两种粉床熔融工艺制备试样,并结合表面形貌观察 (SEM)、显微组织分析、显微硬度测试及单轴拉伸实验,全面评估了工艺 - 组织 - 性能之间的关系。研究表明,SLM 由于冷却速率高,形成以 α' 马氏体为主的细小组织,整体表现出更高的硬度与强度但延性较低;而 EBM 在高温预热粉床条件下成形,获得以片层 α 相和先前 β 晶界为特征的组织,其强度略低于 SLM,但各向异性相对温和。从成形方向看,两种 AM 材料均表现出明显的方向依赖性,其中 45° 方向的屈服与抗拉强度普遍最高。SLM 表面附着的半熔融颗粒尺寸较小 (约 10~40µm) 且分布相对均匀,而 EBM 表面存在更大尺寸的半熔融粉末颗粒 (约 20~70µm),导致其表面粗糙度显著高于 SLM;因此粉末粒径与能量输入方式是造成 EBM 表面更粗糙的主要原因,该差异也可能进一步影响其力学响应与服役性能。Metalnikov 等在模拟体液中测得 EBM 点蚀电位 1.1V (SLM0.8V),归因于 β 相体积分数高且表面粗糙度 Ra=8.6 μm;尽管粗糙度增大,EBM 氧化膜完整性更优。Bandekhoda 等电化学阻抗显示弧半径 1.338 MΩ・cm²,约为 SLM (0.761 MΩ・cm²) 两倍,证实其氧化层电阻更高。生物活性测试中,表面 β 相诱导羟基磷灰石沉积,Ca / P=1.87;SLM 马氏体结构抑制矿化,Ca/P 仅 1.46。

2.3 成型精度与缺陷控制
尽管增材制造具备高度几何自由度,成型精度不足与缺陷残留仍是其临床转化的关键瓶颈。Zheng 等系统研究了 SLM 钛合金多孔支架的精度与孔隙缺陷,在激光功率 200~250W、扫描速度 1000 ~ 1500 mm・s⁻¹、层厚条件下,将体积能量密度锁定于 80 ~ 100 J・mm⁻³,实现孔隙率 65~75%、致密化率 99.2%,未熔颗粒 (PMCs) 面积分数 < 2%;薄层与适中扫描速度协同抑制熔池飞溅及球化,200~400µm 定向孔径显著促进骨长入。Bai 等对比 EBM 与 SLM 缺陷形成机制,指出 EBM 的 10⁻⁴Torr 真空与 700°C 预热降低氧化倾向,冷却速率 10~102°Cs 远低于 SLM (10³ ~ 10³℃・s⁻¹),抑制马氏体相变微裂纹;通过电子束线偏移 200µm 与 50µm 层厚,EBM 获得 5~8% 规则连通孔隙,优于 SLM 的 8~12% 随机缺陷。MartinBezuidenhout 等在 SLM 制备 Ti6Al4V 中,以 175~200W、600~800 mm・s⁻¹ 参数组合将孔隙率降至,并同步实现万古霉素可控释放;后处理 20kHz 超声振动彻底去除局部热积累导致的 PMCs,成型精度达 ±0.05mm,满足复杂多孔精准制造要求。Sun 等采用 EBM 定制钛合金椎体,经电子束能量密度优化后层间未熔合缺陷显著减少,孔隙率稳定于 6~8%,孔径 350~500µm;植入后影像评估显示界面匹配精度 ±0.15mm,26 周骨 - 植入物接触率 (BIC) 达 57%,较传统植入物 (28%) 提升超过一倍。
2.4 力学 - 生物性能平衡难题
增材制造虽可定向调控钛合金力学性能,但同步实现力学适配与骨整合增强仍是当前的核心难题。Luo 等以 SLM 成形 TNZTS 合金,经 1200°C 固溶促使薄壳亚稳 S1 相球化为 S2 相,获得屈服强度 978MPa、延伸率 10.4%、弹性模量 64.2GPa 的强韧匹配;Si 掺杂进一步提升成骨细胞增殖活性,优于 Ti6Al4V,为多功能一体化设计提供新思路。Chen 等针对 EBM 多孔钛,采用 650°C 预热并优化双峰粉末粒径,抑制 “粉末吹飞”,使孔隙连通率 > 95%;所得支架弹性模量与松质骨一致,抗压强度 250MPa,体内骨长入率较常规 EBM 提升 30%,在骨盆肿瘤重建中展现应用潜力。Yin 等利用紫外光对 3D 打印多孔钛进行表面功能化,在维持 850MPa 抗压强度前提下,提高表面亲水性及细胞相容性;兔髁突缺损模型显示,紫外组骨 - 植入物接触率由 35% 升至 62%,矿化骨比例增加 40%,证实表面改性可协同优化力学与生物性能。Duan 等以棋盘扫描策略调控 LPBF 热循环,抑制脆性相析出,保留纳米 α'' 马氏体,使 12Mo-6Zr-2Fe 屈服强度达 1026MPa、延伸率 12.7%(传统单道 <5 %),弹性模量降至;表面自组装 TiO₂+Nb₂O₅纳米氧化膜将溶液中腐蚀电流密度降至 0.1 μA・cm⁻²,成骨分化效率较 Ti6Al4V 提升 1.8 倍,突破高强 β- 钛合金 “强度 - 脆性 - 生物相容” 互斥瓶颈。综上所述,这些研究表明,通过相转变调控、孔结构优化、表面功能化及热循环再设计等手段,可在局部范围内突破传统 “高强 - 低模量 - 高生物活性” 三者难以兼得的瓶颈,但要在同一体系中实现力学性能与骨整合能力全面且长期的平衡仍需进一步探索。
3、增材制造钛合金在骨科中的应用
3.1 髋关节假体以及髋臼骨折固定的植入物定制
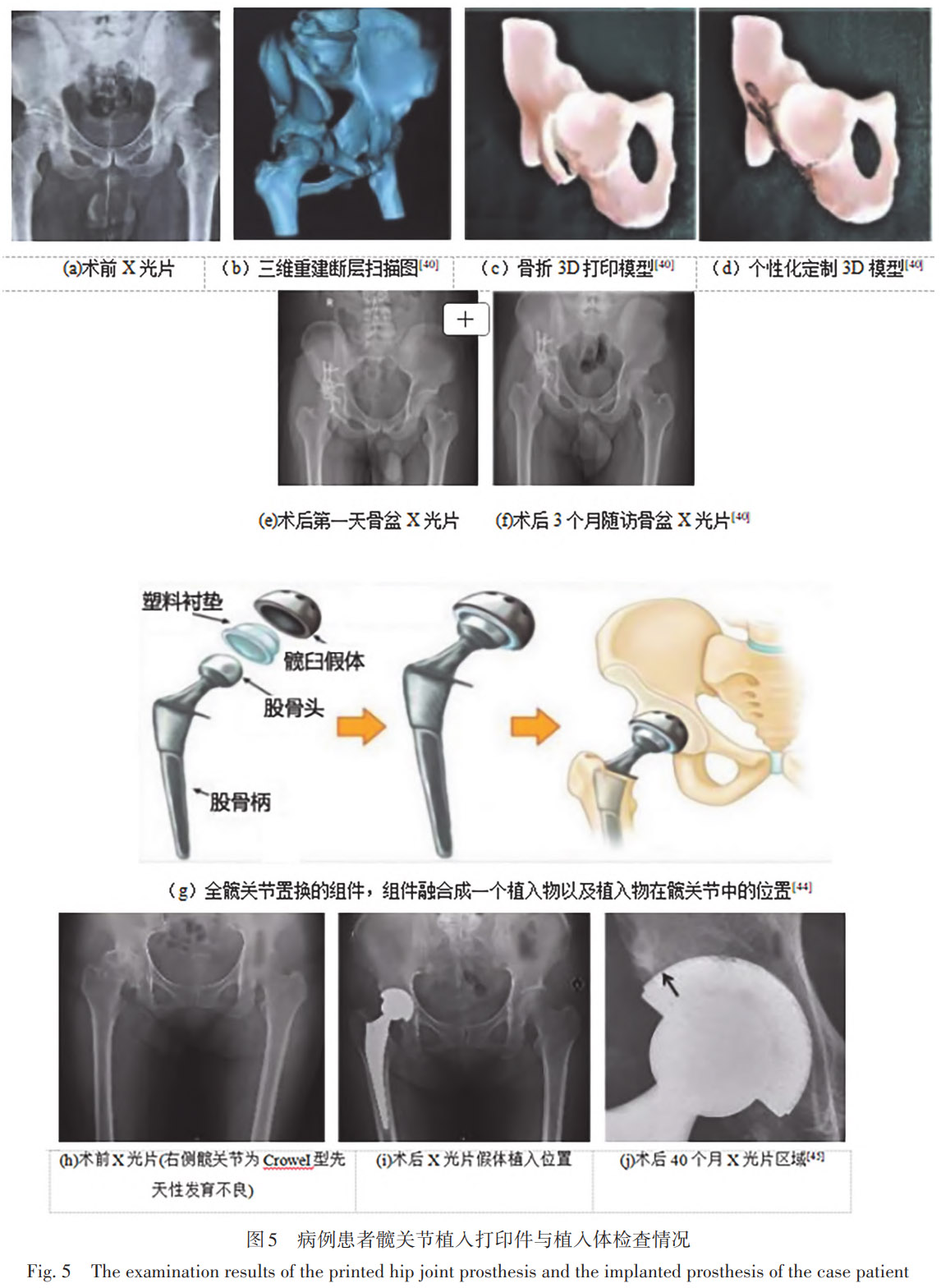
增材制造钛合金已用于髋、膝关节置换,可依据个体解剖定制假体,提升匹配度并加速术后康复。Tomaževič等采用 SLM 为髋臼骨折患者定制钛合金接骨板:术前 3D 复位模拟优化板形与刚度分布,术后骨折线位移较传统组降低 30% (均值 < 1.5mm),孔隙率精准设定于 15~20%,屈服强度≥850MPa,兼顾机械稳定性与骨长入需求。Drobniewski 等通过回顾性长期随访方法,分析了 1999-2010 年间 315 名患者、共 351 个采用钛合金 LCup 多孔覆层髋臼组件的全髋关节置换 (THA) 病例,使用 MAP 评分、VAS 疼痛量表及 X 线影像评估其至少 14 年的临床与影像学结果。发现虽然手术后疼痛与功能均显著改善,但长随访中有 20.5% 的病例出现髋臼杯松动,总体 20 年生存率仅 73.79%,提示该钛合金螺纹杯在长期稳定性方面存在显著风险,得出结论:L-Cup 所采用的 “先敲击再旋入” 的固定位面技术并未在长期表现中成功,未来需要改进设计与手术方式。结合骨科实际应用分析,发现钛合金螺纹杯结构与未封闭的螺钉孔易产生聚乙烯磨损碎屑并导致严重骨溶解 (在松动杯中达 78%),削弱植入物的长期生物固定性;螺纹结构在长期中表现出较高迁移率和松动率;此外,L-Cup 使用的多孔等离子喷涂钛层虽可促进骨结合,但其长期稳定性不足以抵御磨损颗粒病及反复微动,从而导致较高翻修率。Ikumapayi 等采用有限元分析 (FEA) 方法,在 ANSYS 软件中建立了股骨模型,对 316L 不锈钢和钛合金 (Ti-6Al-4V) 在 2300N 载荷下的力学行为进行了模拟与比较。发现在多种力学指标 (如剪切应变、等效应力、总变形等) 对比中,钛与不锈钢的复合材料在多项性能上优于单一材料,尤其在抗剪切应变和抗变形方面表现更佳,说明复合材料能更好平衡两者的优缺点,更适合作为骨科植入材料。钛合金在骨科应用中的缺点主要包括:弹性模量仍高于人骨,易导致应力屏蔽;耐磨性较差,易产生磨损碎屑;剪切强度低;成本较高;加工与焊接工艺复杂;部分合金 (如含钒、铝) 可能释放离子,引起组织毒性或过敏反应;长期使用中可能出现疲劳断裂和局部腐蚀风险。Zhang 等以 SLM 制备髋臼后柱多孔钛板,孔径 300~500µm、连通率 > 95%,表观模量≈30GPa,接近松质骨,显著缓解应力遮挡;12 个月随访 Harris 评分提高 18%,无松动或骨吸收。Stoffelen 团队针对严重髋臼缺损设计出 SLM 仿生多孔假体,孔隙率 40%、小梁厚 0.3mm,压缩强度 ≥600 MPa;年随访实现骨性融合,疼痛缓解,无应力遮挡性骨丢失。Arabnejad 等基于患者 CT 构建有限元模型,通过多尺度拓扑优化确定全多孔股骨柄密度分布,SLM 成形后孔隙率 70%、孔径 500µm,弹性模量可调;体外实验显示,较实心柄骨吸收量减少 75%,Gruen 区 7 骨丢失率由 27% 降至 8%,区 6 由 14% 降至 2%,在维持强度的同时显著改善骨整合,为降低应力屏蔽提供新范式,围绕人工髋关节在人体内长期承受高载荷、复杂生物力学作用及摩擦磨损环境这一核心应用需求,既有研究从材料理论评述与临床实践两个层面逐步展开。Aherwar 等与 Singh 等从宏观材料体系出发,系统阐明了不锈钢、钛合金、钴基合金以及陶瓷、高分子及其复合材料在股骨头、髋臼杯和股骨柄等关键部位中的服役特性,指出人工髋关节失效主要源于磨损碎屑诱发的生物反应、金属离子释放、应力遮挡效应及材料疲劳等多重因素。其中,钴基合金凭借较高的强度和疲劳性能以及依赖 Cr₂O₃钝化膜形成的优异耐磨耐腐蚀能力,更适用于承载与摩擦集中的功能部位;而在聚合物体系中,UHMWPE 虽具备良好的减震与耐磨特性,但仍受限于磨损和蠕变问题,相比之下,PEEK 及其复合材料在降低磨损率和改善力学匹配方面展现出更突出的综合优势。上述研究从理论层面揭示了单一材料难以同时满足人工髋关节对力学性能、生物相容性与长期稳定性的多重要求,强调了多材料协同设计的必要性。刘晨等将这一材料设计理念落实于临床实践,通过对标准化 3D 打印多孔钛合金髋臼杯全髋关节置换患者的中期随访研究证实,类骨小梁结构与合理孔隙参数能够有效促进骨长入,显著改善术后疼痛与功能恢复,并在中期随访内实现 100% 的髋臼杯存活率,体现出良好的初始与长期稳定性。综合来看,从材料理论分析到临床循证结果的层层铺陈表明,以高性能金属为骨架、结合多孔结构优化及聚合物基复合与纳米增强策略的协同设计,是提升人工髋关节长期服役性能与临床可靠性的关键发展方向。
3.2 椎间融合器创新设计
增材制造为椎间融合器提供拓扑自由度,可在保证生物相容性的同时实现机械适配。王彦金等采用 SLM 成形颈椎融合器,外层孔隙率 40%、内层 70%,经 900°C/150MPa 热等静压后致密度自 98.5% 升至 99.6%;弹性模量 4.5GPa,匹配松质骨,成型精度 ±0.1mm。33 例患者 2 年随访沉降率仅 3%。Ji 等采用随机对照试验 (RCT) 对 36 例单节段腰椎退变患者进行对比,其中 19 例使用 3D 打印钛合金 Ti6Al4V 椎间融合器,17 例使用 PEEK 融合器,通过术前与术后 VAS、ODI 评分及 X 线 / CT 影像评估其有效性、安全性与植入物稳定性。研究结果显示,3D 打印钛合金融合器组术后疼痛与功能改善显著,并且在 3-26 个月随访中无一例移位或螺钉松动,明显优于 PEEK 组 (17.6% 移位、5.9% 螺钉松动),结果表明:3D 打印钛合金融合器具有良好生物相容性、力学稳定性与促进骨长入能力,是后路腰椎融合术的有效和安全选择。在骨科应用下,传统钛合金的性能不足:由于弹性模量明显高于椎体骨组织,会产生应力遮挡,导致融合器沉降风险增加,这一点是长期使用金属融合器的生物力学缺陷;此外,金属在传统加工方式下表面光滑,表面骨结合能力不足,可能影响骨融合。因此强调通过 3D 打印构建高达 80% 孔隙率、类松质骨结构及粗糙表面,正是为克服传统钛合金在骨科应用中 “高模量导致沉降” 和 “表面骨整合不足” 的缺点,并提升植入物生物学性能。Shuai 等基于有限元分析 (FEA) 方法,构建了符合真实解剖结构的 L4L5 腰椎后路椎间融合 (PLIF) 模型,对比评估了 3D 打印多孔超低弹性模量 Ti-24Nb-4Zr-8Sn (Ti2448) 融合器、多孔 Ti-6Al-4V (Ti64) 融合器与传统 PEEK 融合器在多种生理工况下的生物力学行为。研究通过比较椎间活动度 (ROM)、椎弓根钉棒系统应力、融合器 - 终板界面应力及界面微动等关键指标,发现两种多孔钛合金融合器整体稳定性优于 PEEK,其中低弹性模量 Ti2448 融合器在降低终板界面应力、改善应力分布及减少沉降风险方面表现最为突出,其力学响应更接近人体骨组织,有利于长期骨整合。Sun 等围绕颈椎前路椎间融合术 (ACDF),采用有限元分析 (FEA) 方法构建了正常颈椎模型,分别植入 ZK60 镁合金融合器、Ti-6Al-4V 钛合金融合器的手术模型,并在屈曲、伸展、侧弯和轴向旋转等工况下系统比较了活动度 (ROM)、融合器变形、融合器及骨移植物应力以及终板 - 融合器界面应力;在此基础上,进一步基于受力特征对 ZK60 融合器进行晶格拓扑优化设计并进行力学验证。结果表明,与钛合金融合器相比,ZK60 融合器可在保持颈椎整体稳定性的同时显著降低融合器及终板界面应力,减弱应力遮挡效应,并提高骨移植物所受的力学刺激 (平均提高约 27.7%),从而更有利于骨融合;而经晶格拓扑优化后的多孔 ZK60 融合器在进一步降低结构刚度和界面应力的同时,表现出更优的生物力学性能。作者据此认为,ZK60 及其晶格优化结构在降低沉降风险、促进骨融合方面具有明显优势,是一种具有应用潜力的颈椎融合器设计方案。McGilvray 等通过采用动物模型实验方法,在绵羊腰椎融合模型中直接比较了 3D 打印多孔钛合金 (PTA)、聚醚醚酮 (PEEK) 以及等离子喷涂多孔钛涂层 PEEK (PSP) 三种椎间融合器的性能。研究通过生物力学测试、微 CT 扫描和组织形态计量学分析,发现 PTA 在骨长入、生物力学稳定性 (如降低运动范围、提高刚度) 以及骨整合方面均显著优于 PEEK 和 PSP,尤其在 16 周时表现出更强的骨整合能力和结构稳定性。Makino 等通过一项临床病例系列研究,比较了使用钛涂层聚醚醚酮 (TCP) 笼与三维多孔钛合金 (PTA) 笼进行后路腰椎椎间融合术 (PLIF) 后短期 (≤1 年) 的影像学与临床结局。研究方法包括对 63 例患者进行回顾性分析,评估融合状态、终板囊肿形成、融合器沉降及患者报告的生活质量 (基于 JOABPEQ 问卷)。结论显示,两组患者在术后 1 年的融合率与生活质量改善方面无显著差异,但 PTA 笼组在术后 6 个月的终板囊肿形成和融合器沉降程度显著低于 TCP 笼组,表明 PTA 笼在早期固定和抑制局部骨吸收方面更具优势。文中指出钛合金作为融合器材料的缺点主要包括:其刚度高于骨骼,可能导致应力屏蔽效应,进而影响骨愈合并增加融合器沉降风险;此外,钛涂层在植入过程中可能发生剥离,产生的磨屑可能引发炎症反应,促进终板囊肿形成与扩散。Donaldson 等分析了 50 例使用 3D 打印多孔钛合金 (3D Ti) 融合器行腰椎前路或侧路椎间融合手术的患者资料 (共 66 个手术节段)。依据 Gruskay 标准评估融合情况,并按 Marchi 分级判断融合器沉降。结论表明,3D 打印钛合金融合器在腰椎前路与侧路融合术中总体沉降率为 3.03%,再手术率为 1.5%,显著低于文献报道的传统 PEEK 或实心钛合金融合器的数据。

3.3 下颌骨重建
增材制造可精准匹配下颌骨复杂解剖,实现钛合金植入物个体化修复。Xue 等以有限元优化 3D 打印钛板 (16mm×2.8mm,10 枚螺钉),应力分布均匀且避免屏蔽;78 岁成釉细胞瘤复发患者术后 CT 显示贴合良好,咬合功能恢复,长期随访无板断裂或螺钉松动。Zhao 等采用 SLM 成形网状下颌假体,ANSYS 疲劳分析表明,0.5mm 丝径可承受 4 次循环,丝径超过 6 ×10⁵次仍完整;比格犬半侧缺损模型中假体无需塑形即精准贴合,6 个月 CT 显示下颌形态与颞下颌关节稳定,无肝肾毒性。Shi 等人通过有限元分析 (FEA)、静力学分析、金相组织与硬度测试 (358±14HV)、断口 SEM 分析等多维方法,对一例在体内使用 34 个月后发生断裂的个体化 Ti-6Al-4V 下颌重建板进行系统失效研究。FEA 显示植入板在咀嚼时承受的最大拉应力约为 392.6MPa,接近材料 510MPa 的疲劳强度,安全系数仅 1.3,且应力高度集中于 S5 螺孔附近,这是断裂最初发生的部位。金相分析表明材料致密度达 99.8±0.05%,但仍存在微孔及 α/α'β 组织,使局部成为疲劳裂纹萌生点;断口 SEM 显示典型的疲劳条纹、解理台阶和韧窝,证实其为高周疲劳主导的混合脆 - 韧断裂模式。此外,裂纹内部检测到 Ca/P/O 沉积和生物液诱导的氢脆迹象,进一步加速裂纹扩展。同时指出,在骨科应用中 Ti6Al-4V 的主要缺点在于:其弹性模量 (113.8GPa) 远高于皮质骨 (13.7GPa),易导致应力屏蔽;疲劳强度有限,在长期复杂咬合力作用下易发生疲劳裂纹;此外 SLM 制备的植入物表面仍可能存在微孔、几何薄弱区及应力集中,均显著降低在体内服役寿命。Dündar 等人采用有限元分析方法,对比了钛合金固定板与镍钛形状记忆钉治疗下颌骨骨折的生物力学性能。发现在 200N 咬合力作用下,NiTi 形状记忆钉 (尤其是三钉且中央钉呈 + 30° 角的最佳配置) 产生的最大应力 (67.16MPa) 显著低于钛板 (单板 194.62MPa,双板 157.47MPa),且两者产生的骨块位移均处于利于骨愈合的微动范围 (0.1–0.8mm) 内,表明 NiTi 钉在提供足够稳定性的同时,能更优地分散应力,是钛板的一种有前景的替代方案。且指出钛合金植入物主要存在以下缺点:其刚性结构及螺钉孔易导致应力集中和应力屏蔽,可能引发骨吸收;临床并发症较多,包括植入物可触及、冷敏感,二次手术移除率高达 10%–23.4%,感染率约 3%–23%;长期生物相容性方面,存在金属离子释放、潜在过敏反应以及在特定环境下腐蚀的风险。Almudarris 等对 30 例下颌缺损行激光粉末床熔融定制 Ti6Al4V 植入并联合软组织移植,12 个月存活率 96.7%,咀嚼效率提高 40%,语言清晰度增加 30%,85% 患者美学评价 “优秀”,仅 2 例轻度感染、1 例松动。Hijazi 等以 SLM 构建单位晶胞 1mm、支柱 350~450µm 的简单立方多孔 Ti6Al4V,弹性模量约 20~30GPa,与皮质骨匹配;疲劳模拟于 50~100N 咀嚼载荷下寿命 4~119 年,植入后疲劳强度翻倍。梯度结构兼顾力学适配与骨整合,为下颌骨缺损提供个体化解决方案。
4 结论与展望
钛合金以其高比强度、优异生物相容性与自钝化耐蚀能力,成为突破传统金属 “力学失配 - 生物惰性” 瓶颈的理想骨科植入材料。选区激光熔化 (SLM) 与电子束熔化 (EBM) 通过逐层累加策略,实现解剖级几何复现与孔隙特征精确控制,分别在成形精度及组织亲和方向形成互补。临床证据已证实 3D 打印钛合金在髋、脊柱与颌面修复中的安全性、力学适配性与功能重建效能。未来研究需聚焦于成分 - 结构协同设计,构建模量梯度多孔框架并耦合生物活性涂层,以同步降低应力屏蔽、促进骨整合;另一方面,需攻克增材过程孔洞、未熔颗粒与表面粗糙度缺陷,通过多参数耦合优化与后处理闭环控制,保障复杂植入物在长期生理载荷下的疲劳可靠性与化学稳定性。推动个性化钛合金植入物向标准化、规模化演进,集成人工智能算法、影像逆向建模与仿生拓扑优化,建立高保真、快响应的临床定制平台,将是实现精准骨科修复的重要方向。
参考文献
[1] 李启荣,李文博,牛楚涵,等。骨科用钛合金表面改性技术与生物相容性研究进展 [J]. 钛工业,2021,38 (5):41-48. Li Qirong, Li Wenbo, Niu Chuhan, et al. Research Progress on Surface Modification Technology and Biocompatibility of Titanium Alloy for Orthopedics [J]. 2021, 38 (5): 41-48.
[2] 宋博,安明宇,王红阳,等。固溶冷却方式对新型高强近 β 钛合金 Ti-5321 微观组织及力学性能的影响 [J]. 聊城大学学报 (自然科学版), 2024, 37 (3): 53-61. Song Bo, An Mingyu, Wang Hongyang, Wang Yisen, Zhen Jinming. Effect of Cooling Method After Solution on Microstructure and Mechanical Properties of New Near-β Ti Alloy Ti-5321 [J]. Journal of Liaocheng University (Natural Science Edition), 2024, 37 (3): 53-61.
[3] 宋博,安明宇,倪俊杰,等。浸泡温度和时间对海洋结构钛合金耐蚀性能的影响 [J]. 聊城大学学报 (自然科学版),2024,37 (6):62-70. Song Bo, An Mingyu, Ni Junjie, et al. Effect of Immersing Temperature and Duration on Corrosion Resistance of Ti Alloy in Marine Field [J], Journal of Liaocheng University (Natural Science Edition), 2024, 37 (6): 62-70.
[4] 张云龙,董鑫焱,翟梓棫,等. Er₂O₃微粒掺杂对 TC4 钛合金微弧氧化涂层组织和耐磨性的影响 [J]. 稀有金属,2024,48 (8):1120-1131. Zhang Yunlong, Dong Xinyan, Zhai Ziyu, et al. Microstructure and Wear Resistance of MAO Coatings of TC4 Alloy with Different Er₂O₃ Doping Amounts [J]. 2024, 48 (8):1120-1131.
[5] 杜忠旭,尹贻彬,宋博,等。微弧氧化制备医用钛合金生物复合涂层研究进展 [J]. 聊城大学学报 (自然科学版), 2025, 38 (3): 404-410. Du Zhongxu, Yin Yibin, Song Bo, NI Junjie, DI Heyang, LIU Zhiwen. Research progress of biocomposite coatings on medical titanium alloy prepared by micro-arc oxidation [J]. Journal of Liaocheng University (Natural Science Edition), 2025, 38 (3): 404-410.
[6] Ampadi Ramachandran, Remya, et al. Artificial intelligence and machine learning as a viable solution for hip implant failure diagnosis-Review of literature and in vitro case study [J]. Medical & Biological Engineering & Computing61.6 (2023): 1239-1255.
[7] Wu, Puzhen, et al. Personalization and Precision: Innovative Applications and Future Challenges of Additive Manufacturing in Orthopedic Implants [J]. Journal of Orthopaedic Research, 2025: 1-17.
[8] Lal, Hitesh, and Mohit Kumar Patralekh. 3D printing and its applications in orthopaedic trauma: a technological marvel [J]. Journal of clinical orthopaedics and trauma,2018,9 (3): 260-268.
[9] Ozan S, Lin J, Li Y, et al. Development of Ti–Nb–Zr alloys with high elastic admissible strain for temporary orthopedic devices [J]. Acta biomaterialia, 2015, 20: 176-187.
[10] Daniel Devaraj L, Srinivasan V. Evaluation of Microhardness, Compression, and Flexural Strength for Gyroid Ti-6Al-4V with Different Porosities Fabricated by Direct Metal Laser Sintering Process for Orthopedic Application [J]. Journal of Materials Engineering and Performance, 2025:1-13.
[11] Murr L E, Amato K N, Li S J, et al. Microstructure and mechanical properties of open-cellular biomaterials prototypes for total knee replacement implants fabricated by electron beam melting [J]. Journal of the mechanical behavior of biomedical materials, 2011, 4 (7): 1396-1411.
[12] McMahon, Rebecca E, et al. A comparative study of the cytotoxicity and corrosion resistance of nickel–titanium and titanium – niobium shape memory alloys [J]. Acta biomaterialia, 2012,8 (7): 2863-2870.
[13] Liu Q, Zhang Y, Chen W, et al. Bioactive and fatigue-resistant Ti–Ta alloy by additive manufacturing for orthopedic applications [J]. Smart Materials in Manufacturing, 2025, (3): 100086.
[14] Guo Y, Wu J, Xie K, et al. Study of bone regeneration and osteointegration effect of a novel selective lasermelted titanium-tantalum-niobium-zirconium alloy scaffold [J]. ACS Biomaterials Science & Engineering, 2019, 5 (12): 6463-6473.
[15] Jing Z, Yuan W, Wang J, et al. Simvastatin/hydrogel-loaded 3D-printed titanium alloy scaffolds suppress osteosarcoma via TF/NOX2-associated ferroptosis while repairing bone defects [J]. Bioactive materials, 2024, 33: 223-241.
[16] Xue Pengfei, et al. Superelasticity, corrosion resistance and biocompatibility of the Ti – 19Zr – 10Nb – 1Fe alloy [J]. Materials Science and Engineering: C, 2015 (50): 179-186.
[17] Li J, Zhong H, Cao B, et al. Comparative Study of 3D-Printed Porous Titanium Alloy with Rod Designs of Three Different Geometric Structures for Orthopaedic Implantation [J]. Acta Metallurgica Sinica, 2024, 37 (1):54-66.
[18] Chellappa M, Vijayalakshmi U. Electrophoretic deposition of silica and its composite coatings on Ti-6Al4V, and its in vitro corrosion behaviour for biomedical applications [J]. Materials Science and Engineering: C, 2017, 71: 879-890.
[19] Xie K, Guo Y, Zhao S, et al. Partially melted Ti6Al4V particles increase bacterial adhesion and inhibit osteogenic activity on 3D-printed implants: an in vitro study [J]. Clinical Orthopaedics and Related Research,2019,477 (12): 2772- 2782.
[20] Guo Y, Ren L, Xie K, et al. Functionalized TiCu/ Ti-Cu-N-coated 3D-printed porous Ti6Al4V scaffold promotes bone regeneration through BMSC recruitment [J]. Advanced Materials Interfaces, 2020,7 (6): 1901632.
[21] Gao B, Zhao H, Peng L, et al. A review of research progress in selective laser melting (SLM)[J]. Micromachines, 2022, 14 (1): 57.
[22] Kolamroudi M K, Asmael M, Ilkan M, et al. Developments on electron beam melting (EBM) of Ti-6Al4V: a review [J]. Transactions of the Indian Institute of Metals, 2021, 74: 783-790.
[23] 张云龙,刘德宝,任晓雪,等。增材制造钛合金显微结构调控与表面改性技术的研究进展 [J]. 聊城大学学报 (自然科学版), 2025,38 (4):543-553 ZHANG Yunlong, LIU Debao, REN Xiaoxue, et al. Research progress in microstructure control and surface modification of additive manufacturing titanium alloys [J]. Journal of Liaocheng University (Natural Science Edition), 2025, 38 (4): 543-553.
[24] 张云龙,刘德宝,任晓雪,等。基于 TPMS 结构设计的钛合金增材制造技术的研究进展 [J/OL]. 聊城大学学报 (自然科学版),.2025,38 (6):918-926. ZHANG Yunlong, LIU Debao, REN Xiaoxue, et al. Research progress of titanium alloy additive manufacturing technology based on TPMS structure designs [J]. Journal of Liaocheng University (Natural Science Edition), 2025,38 (6):918-926.
[25] Zhao X, Li S, Zhang M, et al. Comparison of the microstructures and mechanical properties of Ti-6Al-4V fabricated by selective laser melting and electron beam melting [J]. Materials & Design, 2016, 95: 21-31.
[26] Pasang T, Tavlovich B, Yannay O, et al. Directionally-dependent mechanical properties of Ti6Al4V manufactured by electron beam melting (EBM) and selective laser melting (SLM)[J]. Materials, 2021, 14 (13): 3603.
[27] Metalnikov P, Ben-Hamu G, Eliezer D. Corrosion behavior of AM-Ti-6Al-4V: A comparison between EBM and SLM [J]. Progress in Additive Manufacturing, 2022, 7 (3): 509-520.
[28] Bandekhoda M R, Mosallanejad M H, Atapour M, et al. Investigation on the potential of laser and electron beam additively manufactured Ti – 6Al – 4V components for orthopedic applications [J]. Metals and Materials International, 2024, 30 (1): 114-126.
[29] Zheng Y, Han Q, Wang J, et al. Promotion of osseointegration between implant and bone interface by titanium alloy porous scaffolds prepared by 3D printing [J]. ACS biomaterials science & engineering, 2020, 6 (9): 5181-5190.
[30] Bai Y, Gai X, Li S, et al. Improved corrosion behaviour of electron beam melted Ti-6Al – 4V alloy in phosphate buffered saline [J]. Corrosion Science, 2017, 123: 289-296.
[31] Martin Bezuidenhout, Elzaan Booysen, Anton Du Preez van Staden, et al.Selective Laser Melting of Integrated Ti6Al4V ELI Permeable Walls for Controlled Drug Delivery of Vancomycin [J]. ACS Biomaterials Science & Engineering,2018,4 (12): 4412-4424.
[32] Sun Z, Yin M, Sun Y, et al. Customized multilevel 3D printing implant for reconstructing spine tumor: a retrospective case series study in a single center [J]. Orthopaedic Surgery, 2022, 14 (9): 2016-2022.
[33] Luo X, Liu L H, Yang C, et al. Overcoming the strength–ductility trade-off by tailoring grain-boundary metastable Si-containing phase in β-type titanium alloy [J]. Journal of Materials Science & Technology, 2021, 68: 112-123.
[34] Ge Chen, Aikeremujiang Muheremu, Liu Yang, et al. Three-dimensional printed implant for reconstruction of pelvic bone after removal of giant chondrosarcoma: a case report [J].Journal of International Medical Research,2020, 48 (4): 1-10
[35] Yin C, Zhang T, Wei Q, et al. Surface treatment of 3D printed porous Ti6Al4V implants by ultraviolet photofunctionalization for improved osseointegration [J]. Bioactive Materials, 2022, 7: 26-38.
[36] Duan R, Li S, Cai B, et al. A high strength and low modulus metastable β Ti-12Mo-6Zr-2Fe alloy fabricated by laser powder bed fusion in-situ alloying [J]. Additive Manufacturing, 2021, 37: 101708.
[37] Tomaževič M, Kristan A, Kamath A F, et al. 3D printing of implants for patient-specific acetabular fracture fixation: an experimental study [J]. European Journal of Trauma and Emergency Surgery, 2021, 47: 1297- 1305.
[38] Drobniewski, Marek, et al. High Risk of Revision Associated with the L-Cup Titanium Alloy Porous Coated Acetabular Component in Primary Total Hip Arthroplasty: Minimum Follow-Up of 14 Years [J]. Journal of Clinical Medicine, 2025,14 (4 ): 1301.
[39] Ikumapayi, Omolayo M., et al. Finite Element Analysis and Simulation of 316L Stainless Steel and Titanium Alloy for Orthopedic Hip and Knee Prosthetics [J]. Prosthesis,2025, 7 (3): 64.
[40] Zhang H, Guo H P, Xu R D, et al. Surgical treatment outcomes of acetabular posterior wall and posterior column fractures using 3D printing technology and individualized custom-made metal plates: a retrospective study [J]. BMC surgery, 2024, 24: 157.
[41] Stoffelen D V C, Eraly K, Debeer P. The use of 3D printing technology in reconstruction of a severe glenoid defect: a case report with 2.5 years of follow-up [J]. Journal of Shoulder and Elbow Surgery, 2015, 24 (8): e218-e222.
[42] Arabnejad S, Johnston B, Tanzer M, et al. Fully porous 3D printed titanium femoral stem to reduce stressshielding following total hip arthroplasty [J]. Journal of Orthopaedic Research, 2017, 35 (8): 1774- 1783.
[43] Aherwar A., Patnaik A. & Bahraminasab M. Effect of Molybdenum Content on Structure and Properties of a Co-Cr Biomedical Alloy. J. of Materi Eng and Perform, 2019, 28: 6340–6353
[44] Singh, Ranjeet Kumar, and Swati Gangwar. An assessment of biomaterials for hip joint replacement [J]. International Journal of Engineering, Science and Technology, 2021,13 (1): 25-31.
[45] 刘晨,张克,杨滨。标准化 3D 打印多孔钛合金髋臼杯全髋关节置换术的中期疗效 [J]. 陆军军医大学学报,2022, 44 (15): 1538-1541 Liu Chen,Zhang Ke,Yang Bin. Mid-term efficacy of standardized 3D printed porous trabecular titanium acetabular cup in total hip arthroplasty [J]. Journal of Army Medical University, 2022, 44 (15): 15381541
[46] 王彦金,周英杰,王寅,等. 3D 打印多孔钛合金椎间融合器在颈椎前路椎间盘切除植骨融合治疗颈椎病术中的应用 [J]. 中国骨与关节损伤杂志,2023, 38 (1): 1-5. Wang Yanjin, Zhou Ying-jie, Wang Yin, et al Application of 3D print porous titanium alloy intervertebral fusion cage in anterior cervical discectomy and bone graft fusion for treatment of cervical spondylopathy [J].Chin J Bone Joint Injury, 2023,38 (1): 1-5
[47] Jingtao Ji, Guangdong Chen, Jun Miao. Preliminary Application of 3D-Printed Interbody Fusion Devices in the Treatment of Lumbar Degenerative Diseases [J]. 2024. https://doi.org/10.21203/rs.3.rs-4593148/v1.
[48] Huang Shuai, Jin Xuhui, Li Lei, et al. Biomechanical analysis of 3D printed porous extremely-low modulus Ti-24Nb-4Zr-8Sn lumbar interbody fusion cage-A finite element study [J]. Materials Technoloy, 2024, 39 (1): 2345960.
[49] Sun, Jun, et al. A lattice topology optimization of cervical interbody fusion cage and finite element comparison with ZK60 and Ti-6Al-4V cages [J].BMC musculoskeletal disorders,2021,22 (1): 390.
[50] McGilvray, Kirk C., et al. Bony ingrowth potential of 3D-printed porous titanium alloy: a direct comparison of interbody cage materials in an in vivo ovine lumbar fusion model [J]. The Spine Journal, 2018,18 (7): 1250-1260.
[51] Makino, Takahiro, et al. Comparison of short-term radiographical and clinical outcomes after posterior lumbar interbody fusion with a 3d porous titanium alloy cage and a titanium-coated PEEK cage [J]. Global Spine Journal, 2022,12 (5): 931-939.
[52] Christopher Donaldson, Tomislav Santro, Mohammed Awad, et al. 3D-printed titanium alloy cage in anterior and lateral lumbar interbody fusion for degenerative lumbar spine disease [J]. Journal of Spine Surgery, 2024, 10 (1): 22-30
[53] Runqi Xue, Qingguo Lai, Hongyu Xing, et al. Finite element analysis and clinical application of 3Dprinted Ti alloy implant for the reconstruction of mandibular defects [J]. BMC Oral Health, 2024, 24 (1): 95.
[54] Bingjing Zhao, Hong Wang, Changkui Liu, et al. A preliminary study of the mechanical properties of 3Dprinted personalized mesh titanium alloy prostheses and repair of hemi-mandibular defect in dogs [J]. Journal of Biomedical Materials Research Part B: Applied Biomaterials, 2024, 112 (9): e35466.
[55] Shi, Qimin, et al. Failure analysis of an in-vivo fractured patient-specific Ti6Al4V mandible reconstruction plate fabricated by selective laser melting [J]. Engineering Failure Analysis, 2021 (124): 105353.
[56] Dündar, Mehmet Akif, et al. Comparative biomechanical analysis of titanium fixation plates and NiTi shape memory staples for mandibular fracture treatment using finite element method [J]. Biomedical Signal Processing and Control ,2025 (103): 107501.
[57] Ban Ahmed Almudarris, Tanmay Rajput, Virendra Singh, et al. Outcomes of Using 3D-Printed Titanium Implants in Mandibular Reconstruction [J]. Journal of Pharmacy and Bioallied Sciences, 2025, 17: S1529- 1531.
[58] Hijazi, Khaled Marwan Anis. Porous Titanium Alloy Constructs for Mandibular Reconstruction. Electronic Thesis and Dissertation Repository. 2024:10292
[59] 张云龙,刘德宝,孙鹏飞,等。基于稀土掺杂的增材制造钛合金力学性能与微观组织演化机制研究 [J]. 聊城大学学报 (自然科学版),2026,39 . https://doi.org/10.19728/j.issn1
(注,原文标题:增材制造钛合金在骨科中的应用研究进展_张云龙)
tag标签:钛合金,增材制造,骨科植入物,SLM工艺,EBM工艺



